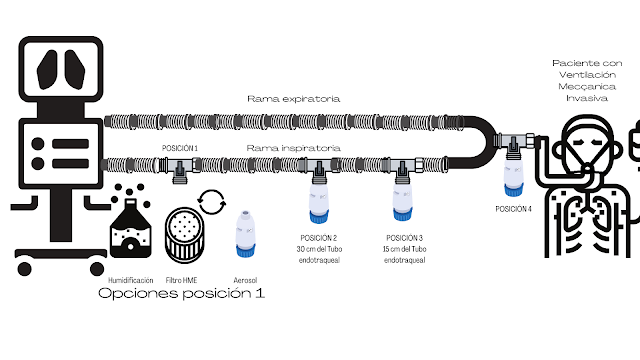
Recibimos un aviso, hay un nuevo mensaje en el buzón del Blog de PreClic 📬Ángela nos contacta para saber "¿Cada cuánto se debe cambiar una cánula de traqueostomia tipo shiley?". Algún PreClic encasillado en cánulas le da al botón rojo 👇🚨y la silla gira... ¡Ángela! tu pregunta está dentro de PreClic.
Vamos a canulear un poco esta tarde... ¡me encanta este royo!
| Foto de canva (https://www.canva.com) |
Bancos de preguntas
Nuestro paso semanal por nuestro amado Preevid esta vez no nos devuelve respuestas. Vamos a seguir avanzando.
Navegamos por Picuida, tenemos una entrada en el banco de preguntas sobre la cuidados en pacientes laringectomizados, pero no aporta respuesta a la pregunta de hoy.
Guías de Práctica Clínica (GPC)
Pasamos al campo de las GPCs y empezamos por GuiaSalud. Esta vez no encontramos información al respecto.
En GIN (metabuscador GPC) no encontramos material relacionado con la frecuencia del cambio de cánula. Y en su homólogo BIGG, no nos ofrece nada nuevo bajo el Sol.
NICE tampoco ofrece guías que nos indiquen el tiempo para el cambio de tubo de traqueostomía. Pero en la Agency for Clinical Innovation (ACI) de Nueva Gales del Sur (Australia) 🦘hemos encontrado una guía de manejo de la traqueostomía muy fresca (2021). En sus recomendaciones para el cambio de cánula completa nos recomienda:
- Que la decisión del cambio de cánula ha de ser tomada por el equipo interdisciplinar. Y debería estar registrado en la historia clínica del paciente (Consenso).
- Los procedimientos locales han de tener en cuenta las recomendaciones del fabricante sobre la frecuencia del cambio de cánula (Consenso).
Revisiones sistemáticas (RS)
No hemos encontrado RS sobre el tema en Cochrane Library.
Bases de datos
Llegados a este punto y según las características de edad en las que se pueden clasificar los estudios vamos a presentar los resultados obtenidos por edad.
Estudios en pacientes pediátricos:
Desde nuestra búsqueda en Pubmed destacamos un estudio de series de casos del 2008 al 2013, de Van Buren en 2014 que presenta buenos resultados en pacientes pediátricos en primer cambio durante el tercer día post quirúrgico, presenta sesgos acordes al tipo de estudio y supone un estudio de mayor repercusión que los consensos o revisiones narrativas.
Y si conocía ya el artículo de primer cambio de cánula en paciente pediátrico al tercer día ¡no se pierda la revisión retrospectiva que concluye que se puede decanular al segundo día! Woods en 2019 realizó este estudio con una muestra de 26 pacientes en el grupo de cambio a los dos días. Así que tomaremos este artículo con precaución, por el tamaño de su población y las características del tipo de estudio.
Ya entrando en la década de los veinte, obtenemos una revisión narrativa de 2020 sobre cuidados de la traqueostomía en pacientes pediátricos. De ella destacamos la referencia al consenso de 2013 de Mitchell y el grupo internacional de ORL pediátrica en 2016, que establecieron el primer cambio entre el quinto y el séptimo día en pacientes pediátricos.
Pero si Cochrane no ha encontrado revisiones sistemáticas, sí que nos ha localizado un ECA de Chorney en 2020, sobre el primer cambio de cánula de traqueostomía en paciente pediátrico. Este estudio relata que el primer cambio no tiene que darse a los siete días como es convenido, sino que a los cuatro días da lugar a menos heridas periostomales, menos sedación y un alta más temprana de los cuidados intensivos. No obstante, este es un estudio muy pequeño (n=15) y deberíamos considerarlo un estudio de interés para desarrollar futuros más potentes.
De vuelta a Pubmed, hemos dado con una GPC de la "American Association for Respiratory Care" de 2021, sobre el manejo en paciente pediátrico, que nos indica que la evidencia de bajo nivel apoya el cambio de una cánula de traqueotomía en el tercer día postoperatorio en pacientes pediátricos sin riesgo de aumento de las complicaciones (nivel de evidencia B). Además, en paciente pediátrico en los cambios rutinarios, las cánulas de traqueotomía deben cambiarse según sea necesario debido a la obstrucción y con regularidad, como mínimo cada 1-2 semanas (nivel de evidencia B).
Nos pasamos a PubMed para hacer una búsqueda, hacernos un "Back to the future" para irnos a 2010, cuando White y sus compañeros escribieron "When to change a tracheostomy tube", entre las razones por las que cambiar una cánula de traqueostomía relatan:
- Primer cambio a los 7 o 14 días de su inserción.
- Cambio para reducir el calibre de la cánula.
- Cambio de rutina cada 60-90 días.
- Mal posicionamiento en tanto a diámetro como a longitud.
- Asincronía entre ventilador y paciente (sospecha de problema de la cánula).
- Pérdidas del balón de neumotaponamiento.
- Roturas de la cánula.
- Para permitir el paso del fibroscopio.
- Cambio del tipo de cánula.
En cuanto al cambio rutinario destaca las variabilidad según las instituciones. Entre las causas para este describe:
- Prevención de granulomas (cada 2 semanas)
- Prevención del bloqueo de la cánula por secreciones.
- Facilitación de la ventilación o el habla.
- Prevención de biofilm (1 mes, en cánulas poliméricas, pero no hay suficientes datos).
Llegados a este punto revisa las recomendaciones de cambio de cánula de los fabricantes:
- Shiley (PVC) 29 días.
- Portex Blue Line (PVC) 30 días.
- Bivona (silicona) 29 días.
- PVC flexible 3-4 meses.
- Cánulas de metal indefinidamente (si no aparecen daños).
Sobre este artículo hay que indicar que es una revisión narrativa sin análisis de los estudios en los que se basa. Por lo tanto, presente un nivel de evidencia bajo. La fecha de su publicación hace que nos tengamos que revisar los datos que presenta y los hemos actualizado con los enlaces que podéis ver en la lista anterior.Otro estudio de cohortes recuperado realizado en 65 pacientes, revisó las diferencias en la colonización de cánulas de traqueostomía comparando cambios de menos de 4 semanas y de más de 4 semanas. En este punto debemos de destacar que la pauta del centro era el primer cambio de cánula entre las semanas 2-4 y posteriormente cada 4-6 semanas, llegando a 3 meses en el entorno domiciliario. Los resultados no encontraron diferencias entre el grupo de menos de 4 semanas y el grupo de más de 4 semanas en tanto a la colonización del dispositivo.
- Los cambios de cánula de traqueostomía de PVC (Shiley) se deben de llevar a cabo en base a la evidencia de los estudios, las recomendaciones del fabricante, el estado clínico del paciente y el consenso del equipo multidisciplinar. La decisión debe quedar registrada en la historia clínica.
- Criterios para cambios de cánula:
- Cambio para reducir el calibre de la cánula.
- Mal posicionamiento en tanto a diámetro como a longitud.
- Asincronía entre ventilador y paciente (sospecha de problema de la cánula).
- Pérdidas del balón de neumotaponamiento.
- Roturas de la cánula.
- Para permitir el paso del fibroscopio.
- En pacientes pediátricos y neonatales:
- La recomendación general del primer cambio es de 5 a 7 días. No obstante, la última evidencia se decanta por cambios tempranos a partir de los 3 días.
- La recomendación general de cambios rutinarios es según clínica o cada 7 -14 días.
- En pacientes adultos:
- Primer cambio: La recomendación general del primer cambio es de 7 a 14 días.
- Cambios rutinarios: cada 28-30 días (pesa la recomendación del fabricante).

.png)

.jpg)